绿色有机合成是有机化学的一个重要领域,“绿色化学”的概念自20世纪80、90年代提出以来,就受到了有机化学家们的广泛关注,尤其自1998年以后,“绿色化学”一词的使用呈线性方式快速增长。近年来,由于开发绿色和可持续方法的潜力,电化学与可见光催化有机合成成为了有机化学的研究热点。437必赢会员中心杜正银、傅颖团队近年来主要开展了过渡金属催化的C-H活化官能化反应研究,结合可见光催化、电化学方法在有机合成中的应用,发展了多种高效、绿色的C-N键、C-C键、C-O键和C-X键的活化和构筑方法,在前期研究工作积累的基础上,受编辑部邀请撰写了关于可见光催化有机反应(Org. Biomol. Chem. 2022, 20, 6721-6740)和二芳基碘盐参与的芳基化反应(Curr. Org. Chem. 2021, 25, 1298-1320)的综述论文各1篇。2023年在炔丙基吲哚与环醚的串联自由基环化反应(J. Org. Chem., 2023, 88, 6374-6381)和自由基Catallani反应研究方面(Adv. Synth. Catal., 2023, 365, 4248-4255)取得了较好成果。近期该团队在过渡金属催化N-杂环化合物合成方法学研究方面又取得了新进展。
2-取代苯并噻唑是一种重要的氮杂环化合物,具有广泛的生物活性,普遍存在于天然产物和药物分子中,由于其特殊的双环体系而受到了广泛的关注。我们利用电化学反应的优点和多组分反应的高效性,用易得原料芳香醛类化合物、丙二睛、2-氨基苯硫酚在电反应条件下高效合成2-取代苯并噻唑,使用电子作为无质量试剂,完全避免了传统化学试剂外部氧化剂的使用,从而消除废物的产生(图1)。
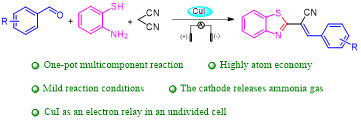
图1 取代苯并噻唑的合成策略
通过优化反应条件,我们共合成了18个目标产物,收率最高91%。为了阐明可能的反应机理,我们设计了一系列的控制实验(图2)和循环伏安实验。首先,标准反应条件下,该反应在空气和氩气气氛中都能顺利进行,以高产率得到目标化合物5a。证明了该反应中涉及电化学阳极氧化,而不是空气中氧气的氧化(图2a)。为了探究反应过程中可能存在的中间体,我们用化合物6a与2-氨基苯硫酚在最优条件下进行反应,分离出79%的目标产物5a。说明该反应过程中涉及苯甲醛与丙二睛发生Knoevenagel缩合反应生成缩合产物1,2-二氰基苯乙烯(图2b)。接着我们进行了自由基捕获实验,利用自由基捕获试剂包括TEMPO、BHT和1,1-二苯乙烯对该反应进行自由基抑制实验,发现该反应被完全抑制,从而表明该反应转化中涉及自由基。通过HRMS检测到了自由基捕获化合物8, 9, 10,表明了反应过程中自由基B与D的存在(图2c)。随后,我们对该反应的实用性进行了研究。首先在标准条件下将底物1a, 2, 3的反应体系进行了克级规模的放大实验,结果以62%的产率得到了1.14 g的克级产物(图2d)。
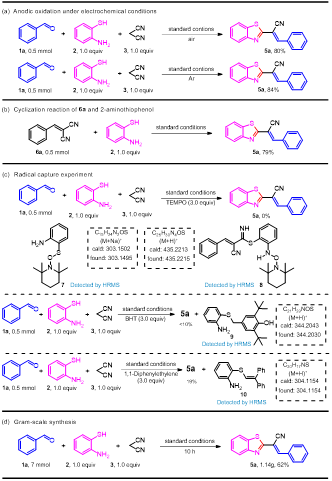
图2 取代苯并噻唑合成的控制实验
根据控制实验结果,我们提出了该反应的可能机理,即碘化亚铜作为电子中继体,催化苯甲醛、2-氨基苯硫酚和丙二腈的一锅三组分反应。在没有外部加热和氧化剂的情况下,在较短的反应时间内获得了一系列2-烯基取代的苯并噻唑。氨气是这个反应的副产物。该方法具有底物范围广,官能团耐受性好,一步反应避免了中间体的分离,具有良好的实用价值,为各种杂环化合物的合成提供了全新的思路。这一成果近期以“Cu-catalyzed, electron-relayed three-component synthesis of 2-alkenylbenzothiazoles with cathode ammonia evolution”为题发表于Green Chemistry(Green Chem. 2023, DOI: 10.1039/D3GC03884J)上.
环状酰亚胺的结构基序经常被发现在各种生物活性分子、多功能材料、农用化学品和聚合物的框架中,此外,这类化合物在调节一些主要已上市药物的功能中发挥着不可或缺的作用。因此,寻找合成环酰亚胺的新策略将具有重要意义,因为它可以为获得结构更新的具有新性质和应用的复杂N-杂环化合物提供新的途径。
二氟卡宾是有机化学领域中非常重要的活性中间体,作为羰基源转化率高、操作简单。我们之前报道了一种构建环化羰基化产物的有效方法,即通过C-H活化和二氟卡宾转移高效合成吲哚-吲哚酮类化合物(Org. Biomol. Chem., 2022, 20, 8120-8124)。最近,我们以邻碘苯甲酰胺和二氟卡宾前驱体反应,通过Pd催化引发N-H键活化和二氟卡宾转移发生[4+1]环加成反应,一步构建了C-C键、C-N键和C=O键,以高产率生成N-取代的邻苯二甲酰亚胺类化合物(图3)。
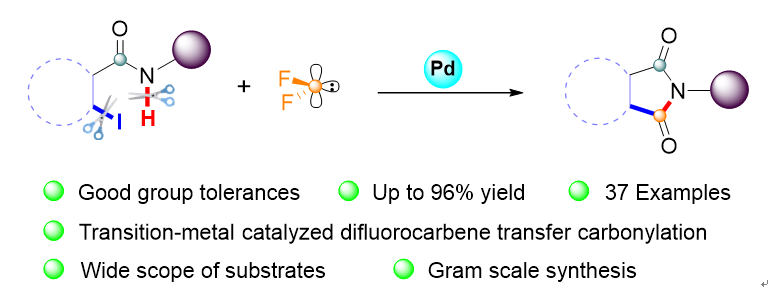
图3 二氟卡宾作为羰基源参与邻苯二甲酰亚胺的合成
通过对催化剂、配体、溶剂、添加剂等反应条件的优化后,在最优条件下我们共合成了43个化合物,收率最高达96%。为了探究反应的机理,我们进行了一系列控制实验:卤素原子的反应活性(图4a)、羰基作用的探讨(图4b)、二氟卡宾的捕获(图4c)、同位素追踪(图4e)。随后,我们又进行了放大实验,得到了克级产物,验证了该反应具有良好的实用性(图4f)。在控制实验的基础上提出了Pd催化循环的可能机理。
该方法具有广泛的底物范围,良好的官能团耐受性和区域选择性,在开发和合成含有环酰亚胺框架的新型类药物化合物方面具有广泛的应用潜力,这是第一个使用二氟卡宾作为羰基源合成N-取代邻苯二甲酰亚胺的例子。该成果近期以“Synthesis of N-substituted phthalimides via Pd-catalyzed [4+1] cycloaddition reaction”为题发表于Chemical Communications (Chem. Commun., 2023, 59, 14839-14842)上。
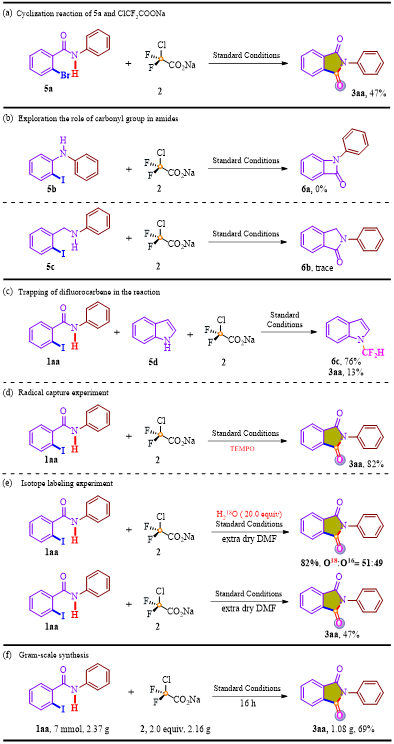
图4 合成邻苯二甲酰亚胺的控制实验
以上研究工作的第一作者为2022级博士研究生虎成贤同学,通讯作者为杜正银教授和傅颖副教授,437必赢会员中心为第一署名单位。该研究得到了国家自然科学基金(21762039, 21762040,22161041)和甘肃省自然科学基金(20JR5RA521)的支持。
甘公网安备62010502000864号 陇ICP备17000462号-1